 |
|||||||
 |
|||||||
La institución desarrolla acciones conducentes al registro, control, fiscalización y vigilancia de la sanidad y calidad de los productos, substancias, elementos, procesos, tecnologías y materiales que se consumen o utilizan en medicina, alimentación y cosmética humanas y del contralor de las actividades y procesos que median o están comprendidos en estas materias.
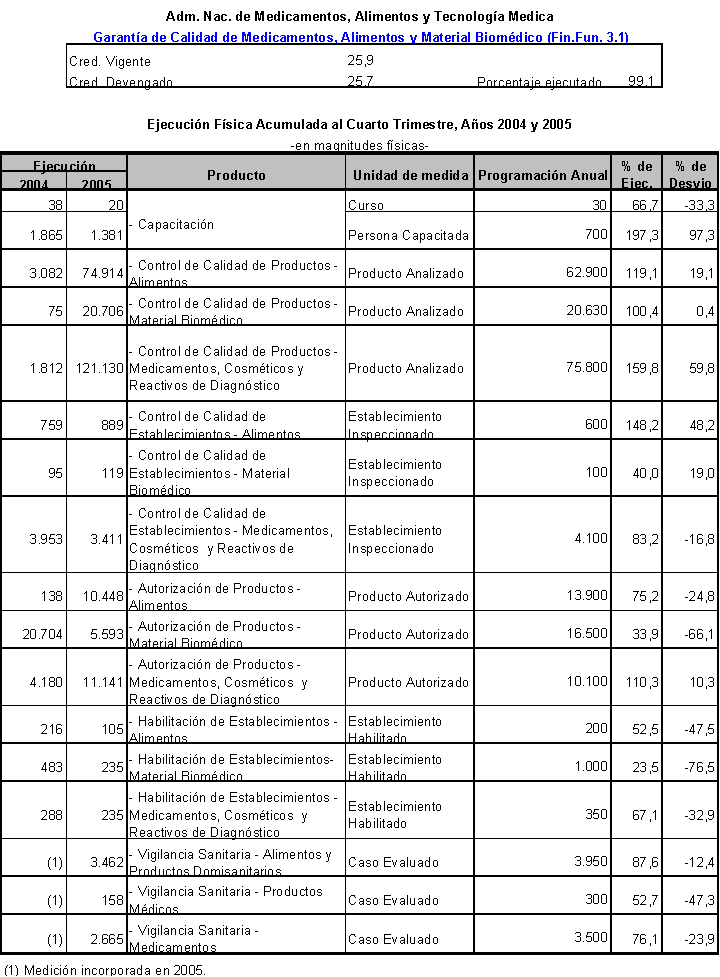
La mayor cantidad de personas capacitadas respecto de lo previsto se debe a la gran convocatoria de profesionales que produjo la presentación de la Guía de Ensayos Clínicos a la sociedad científica. Además tuvo gran número de interesados el curso de Herramientas Estadísticas para Laboratorios y el curso a distancia sobre Buenas Prácticas de Fabricación. Al mismo tiempo profesionales de esta Administración Nacional realizaron capacitación fuera de la institución a requerimiento de organismos provinciales de control en las provincias de Chaco y La Rioja. De los cursos que se desarrollaron durante el último trimestre del año se destacan, el Curso On Line Fiscalización Sanitaria de la Cadena de Comercialización de Medicamentos, el Taller de Capacitación para Investigadores Clínicos en Hematología, el Curso de Control de Esterilidad, el I Taller Nacional sobre Gestión de Accidentes Alimentarios y la Jornada de Capacitación para la Seguridad en la Adquisición de Medicamentos.
Las metas relacionadas al control de calidad de productos se desarrollaron en línea con lo programado y registraron diferencias muy marcadas con respecto a la ejecución del año anterior debido, en parte, al aumento de la demanda.
Debido a que no se contó con el personal necesario en la Dirección de Tecnología Médica, los establecimientos productores de medicamentos, cosméticos y reactivos de diagnóstico ya habilitados no fueron inspeccionados de acuerdo a lo previsto en este período.
Con respecto a la autorización de productos, el rubro material biomédico presenta una notoria disminución con relación a lo ejecutado el año anterior, debido a que está sujeto a nuevas normativas relacionadas con el empadronamiento de empresas fabricantes e importadoras de productos médicos, las cuales han tenido una respuesta tardía al cumplimiento de la obligación de reinscribir sus productos, lo que derivó en la prórroga del vencimiento para realizar el trámite en cuestión y como consecuencia provocó un corrimiento en las metas programadas que también afectará lo programado para el próximo año, en virtud de la prórroga mencionada.
Las acciones destinadas a la habilitación de establecimientos presentaron durante el año una ejecución por debajo de lo programado. En el caso de los establecimientos relacionados a material biomédico, la meta se vio afectada porque el número de inspectores de que se dispone en la actualidad resulta insuficiente.
En general las actividades destinadas a la vigilancia sanitaria no alcanzaron los objetivos debido a que están fuertemente influidas por la cantidad de denuncias provenientes de profesionales y usuarios de manera espontánea, lo que hace poco predecible su comportamiento.
Cabe destacar que los reiterados paros de actividades de profesionales en el Instituto Nacional de Medicamentos (INAME) y en el Instituto Nacional de Alimentos (INAL) afectaron el normal desenvolvimiento de las actividades de esta Administración Nacional.